Nat Med | Multi-omický přístup k mapování integrované nádorové, imunitní a mikrobiální krajiny kolorektálního karcinomu odhaluje interakci mikrobiomu s imunitním systémem
Přestože biomarkery primárního karcinomu tlustého střeva byly v posledních letech rozsáhle studovány, současné klinické pokyny se pro určení doporučení léčby spoléhají pouze na staging nádoru, lymfatických uzlin a metastáz a detekci defektů opravy nesouladu DNA (MMR) nebo mikrosatelitní instability (MSI) (kromě standardního patologického testování). Výzkumníci zaznamenali nedostatek souvislosti mezi imunitními odpověďmi založenými na genové expresi, mikrobiálními profily a nádorovým stromatem v kohortě pacientů s kolorektálním karcinomem z Cancer Genome Atlas (TCGA) a přežitím pacientů.
S postupem výzkumu bylo hlášeno, že kvantitativní charakteristiky primárního kolorektálního karcinomu, včetně buněčné, imunitní, stromální nebo mikrobiální povahy rakoviny, významně korelují s klinickými výsledky, ale stále existuje jen omezené pochopení toho, jak jejich interakce ovlivňují výsledky pacientů.
Aby se rozebral vztah mezi fenotypovou komplexností a výsledkem, tým výzkumníků z Sidra Institute of Medical Research v Kataru nedávno vyvinul a validoval integrované skóre (mICRoScore), které identifikuje skupinu pacientů s dobrou mírou přežití kombinací charakteristik mikrobiomu a konstant imunitního odmítnutí (ICR). Tým provedl komplexní genomickou analýzu čerstvě zmrazených vzorků od 348 pacientů s primárním kolorektálním karcinomem, včetně sekvenování RNA nádorů a odpovídající zdravé kolorektální tkáně, sekvenování celého exomu, sekvenování hlubokého T-buněčného receptoru a genu 16S bakteriální rRNA, doplněné sekvenováním celého nádorového genomu pro další charakterizaci mikrobiomu. Studie byla publikována v časopise Nature Medicine pod názvem „Integrovaný nádorový, imunitní a mikrobiomový atlas rakoviny tlustého střeva“.

Článek publikovaný v Nature Medicine
Přehled AC-ICAM
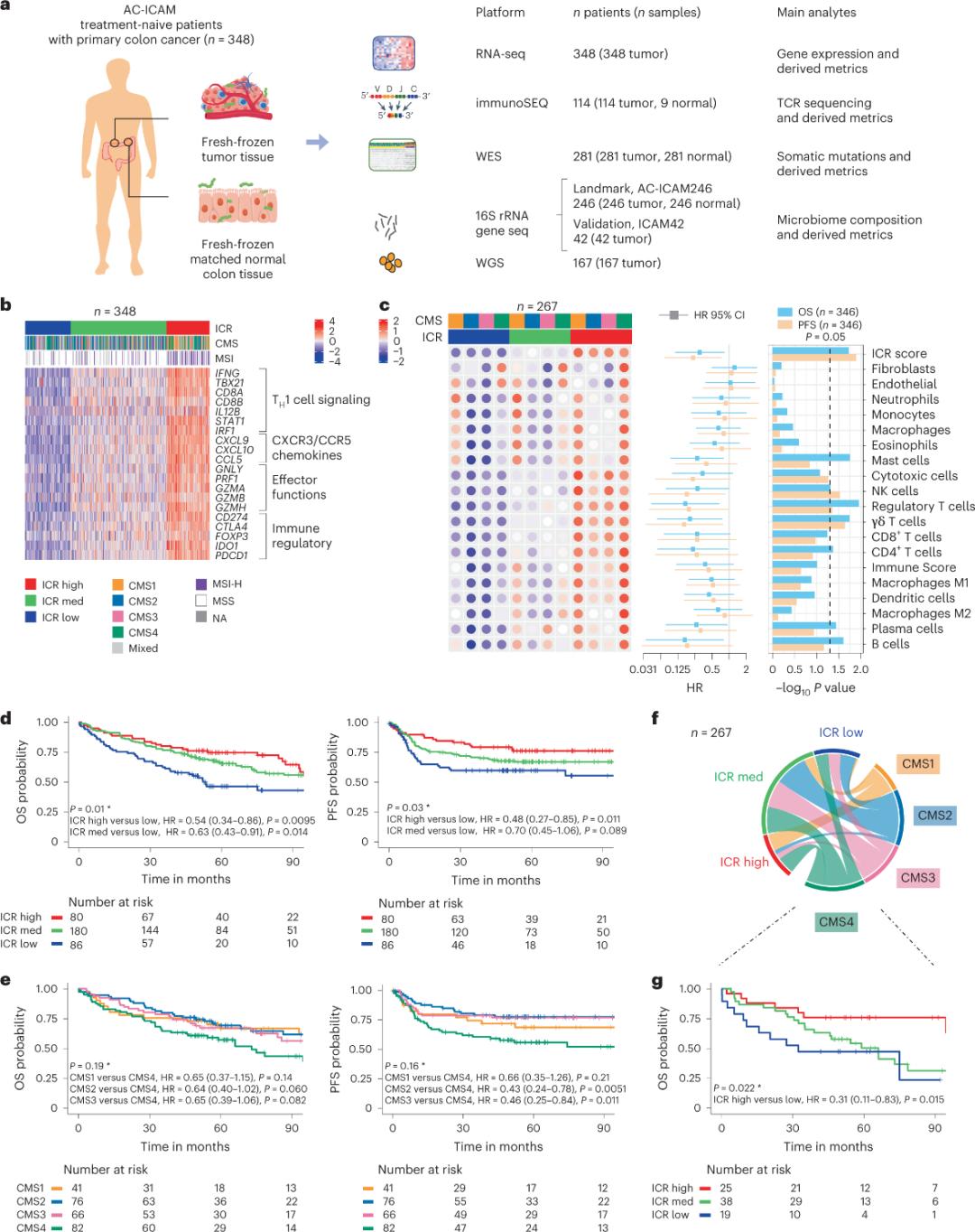
Výzkumníci použili ortogonální genomickou platformu k analýze čerstvě zmrazených vzorků nádorů a porovnatelné sousední zdravé tkáně tlustého střeva (páry nádor-normální tkáň) od pacientů s histologickou diagnózou rakoviny tlustého střeva bez systémové terapie. Na základě sekvenování celého exomu (WES), kontroly kvality dat RNA-seq a screeningu dle inkluzních kritérií byla uchována genomická data od 348 pacientů a použita pro následnou analýzu s mediánem sledování 4,6 roku. Výzkumný tým tento zdroj nazval Sidra-LUMC AC-ICAM: Mapa a průvodce interakcemi imunity-rakoviny-mikrobiomu (obrázek 1).
Molekulární klasifikace pomocí ICR
Výzkumný tým optimalizoval modulární sadu imunitních genetických markerů pro kontinuální imunologickou kontrolu rakoviny, nazývanou imunitní konstanta odmítnutí (ICR), a sloučil ji do 20genového panelu pokrývajícího různé typy rakoviny, včetně melanomu, rakoviny močového měchýře a rakoviny prsu. ICR byla také spojována s imunoterapeutickou odpovědí u různých typů rakoviny, včetně rakoviny prsu.
Nejprve vědci validovali ICR podpis kohorty AC-ICAM pomocí přístupu koklasifikace založeného na genech ICR ke klasifikaci kohorty do tří shluků/imunitních podtypů: vysoký ICR (horké nádory), střední ICR a nízký ICR (studené nádory) (obrázek 1b). Vědci charakterizovali imunitní sklon spojený s konsenzuálními molekulárními podtypy (CMS), což je klasifikace rakoviny tlustého střeva založená na transkriptomech. Kategorie CMS zahrnovaly CMS1/imunitní, CMS2/kanonický, CMS3/metabolický a CMS4/mezenchymální. Analýza ukázala, že skóre ICR negativně korelovalo s určitými drahami rakovinných buněk u všech podtypů CMS a pozitivní korelace s imunosupresivními a stromálními drahami byly pozorovány pouze u nádorů CMS4.
Ve všech CMS byla hojnost podskupin přirozených zabíječských (NK) buněk a T buněk nejvyšší u vysoce imunních podtypů ICR s větší variabilitou u ostatních podskupin leukocytů (obrázek 1c). Imunitní podtypy ICR měly odlišné celkové přežití (OS) a přežití bez progrese (PFS) s progresivním nárůstem ICR od nízké po vysokou (obrázek 1d), což potvrzuje prognostickou roli ICR u kolorektálního karcinomu.
Obrázek 1. Design studie AC-ICAM, imunitně podmíněný genový podpis, imunitní a molekulární podtypy a přežití.
ICR zachycuje nádorem obohacené, klonálně amplifikované T buňky
Pouze menšina T buněk infiltrujících nádorovou tkáň byla hlášena jako specifická pro nádorové antigeny (méně než 10 %). Proto je většina intratumorálních T buněk označována jako bystander T buňky (bystander T buňky). Nejsilnější korelace s počtem konvenčních T buněk s produktivními TCR byla pozorována v subpopulacích stromálních buněk a leukocytů (detekováno pomocí RNA-seq), což lze použít k odhadu subpopulací T buněk (obrázek 2a). V klastrech ICR (celková a CMS klasifikace) byla nejvyšší klonalita imunitních SEQ TCR pozorována ve skupinách ICR-high a CMS subtypu CMS1/imunitní (obrázek 2c) s nejvyšším podílem nádorů ICR-high. Při použití celého transkriptomu (18 270 genů) patřilo šest genů ICR (IFNG, STAT1, IRF1, CCL5, GZMA a CXCL10) mezi deset genů pozitivně asociovaných s klonalitou imunitních SEQ TCR (obrázek 2d). Klonalita TCR měřená pomocí imunosekvence (ImmunoSEQ) korelovala s většinou genů ICR silněji než korelace pozorované s použitím markerů CD8+ reagujících na nádor (obrázek 2f a 2g). Závěrem lze říci, že výše uvedená analýza naznačuje, že podpis ICR zachycuje přítomnost nádorem obohacených, klonálně amplifikovaných T buněk a může vysvětlovat jeho prognostické důsledky.
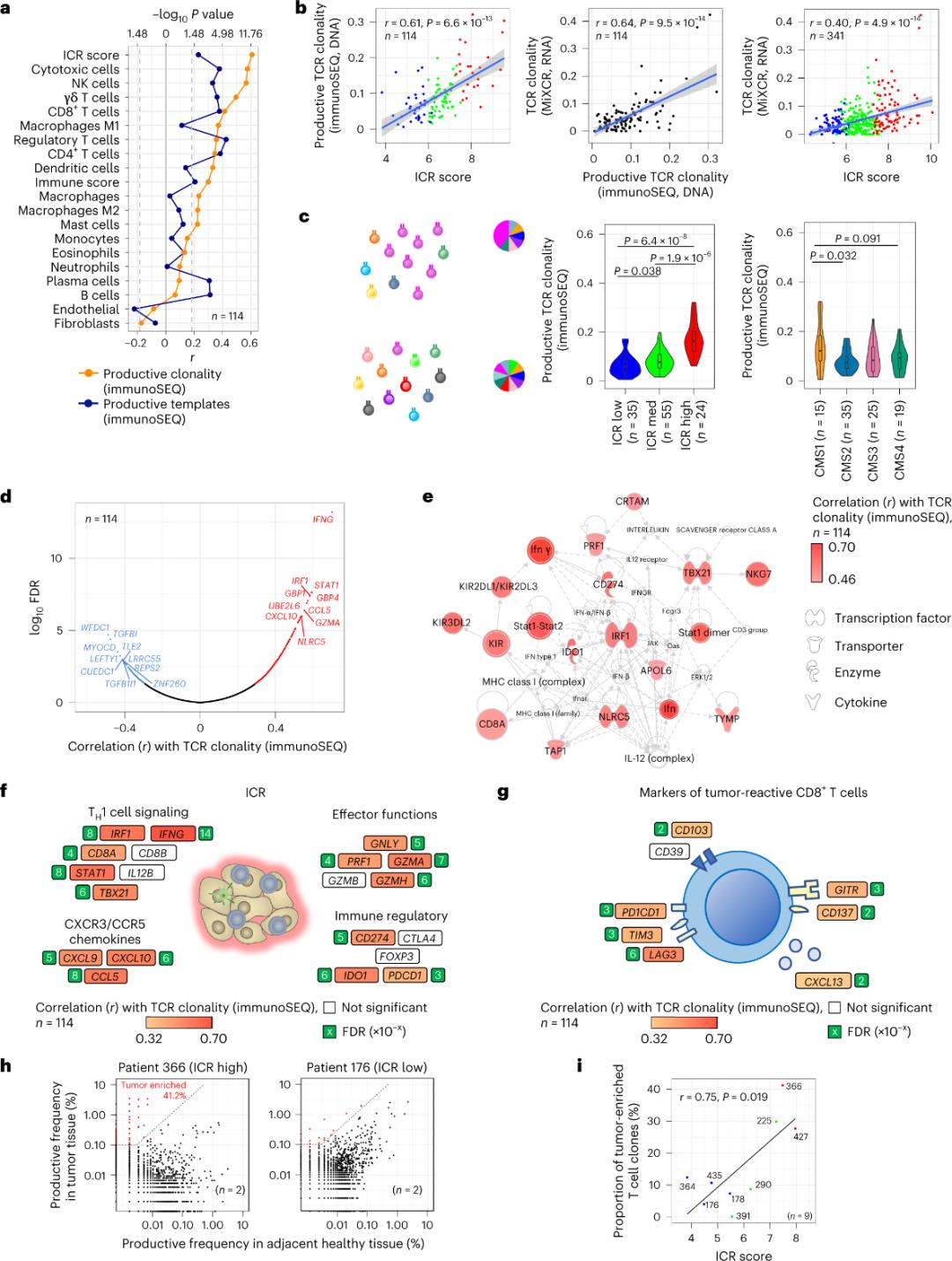
Obrázek 2. Metriky TCR a korelace s imunitně vázanými geny, imunitními a molekulárními podtypy.
Složení mikrobiomu ve zdravých tkáních a tkáních s rakovinou tlustého střeva
Výzkumníci provedli sekvenování 16S rRNA s použitím DNA extrahované ze shodné nádorové a zdravé tkáně tlustého střeva od 246 pacientů (obrázek 3a). Pro validaci vědci dodatečně analyzovali data sekvenování genu 16S rRNA z dalších 42 vzorků nádorů, u kterých nebyla k dispozici shodná normální DNA pro analýzu. Nejprve vědci porovnali relativní početnost flóry mezi shodnými nádory a zdravou tkání tlustého střeva. Clostridium perfringens bylo v nádorech významně zvýšeno ve srovnání se zdravými vzorky (obrázek 3a-3d). Nebyl zjištěn žádný významný rozdíl v alfa diverzitě (rozmanitost a početnost druhů v jednom vzorku) mezi nádorovými a zdravými vzorky a u nádorů s vysokým ICR v porovnání s nádory s nízkým ICR bylo pozorováno mírné snížení mikrobiální diverzity.
Aby se odhalily klinicky relevantní souvislosti mezi mikrobiálními profily a klinickými výsledky, výzkumníci se zaměřili na použití dat ze sekvenování genu 16S rRNA k identifikaci znaků mikrobiomu, které predikují přežití. V rámci studie AC-ICAM246 vědci spustili regresní model OS Cox, který vybral 41 znaků s nenulovými koeficienty (spojenými s diferenciálním rizikem úmrtnosti), nazývaných klasifikátory MBR (obrázek 3f).
V této výcvikové kohortě (ICAM246) bylo nízké skóre MBR (MBR<0, nízké MBR) spojeno s významně nižším rizikem úmrtí (85 %). Výzkumníci potvrdili souvislost mezi nízkým MBR (rizikem) a prodlouženým OS ve dvou nezávisle validovaných kohortách (ICAM42 a TCGA-COAD). (Obrázek 3) Studie prokázala silnou korelaci mezi endogastrickými koky a skóre MBR, která byla podobná v nádorové i zdravé tkáni tlustého střeva.
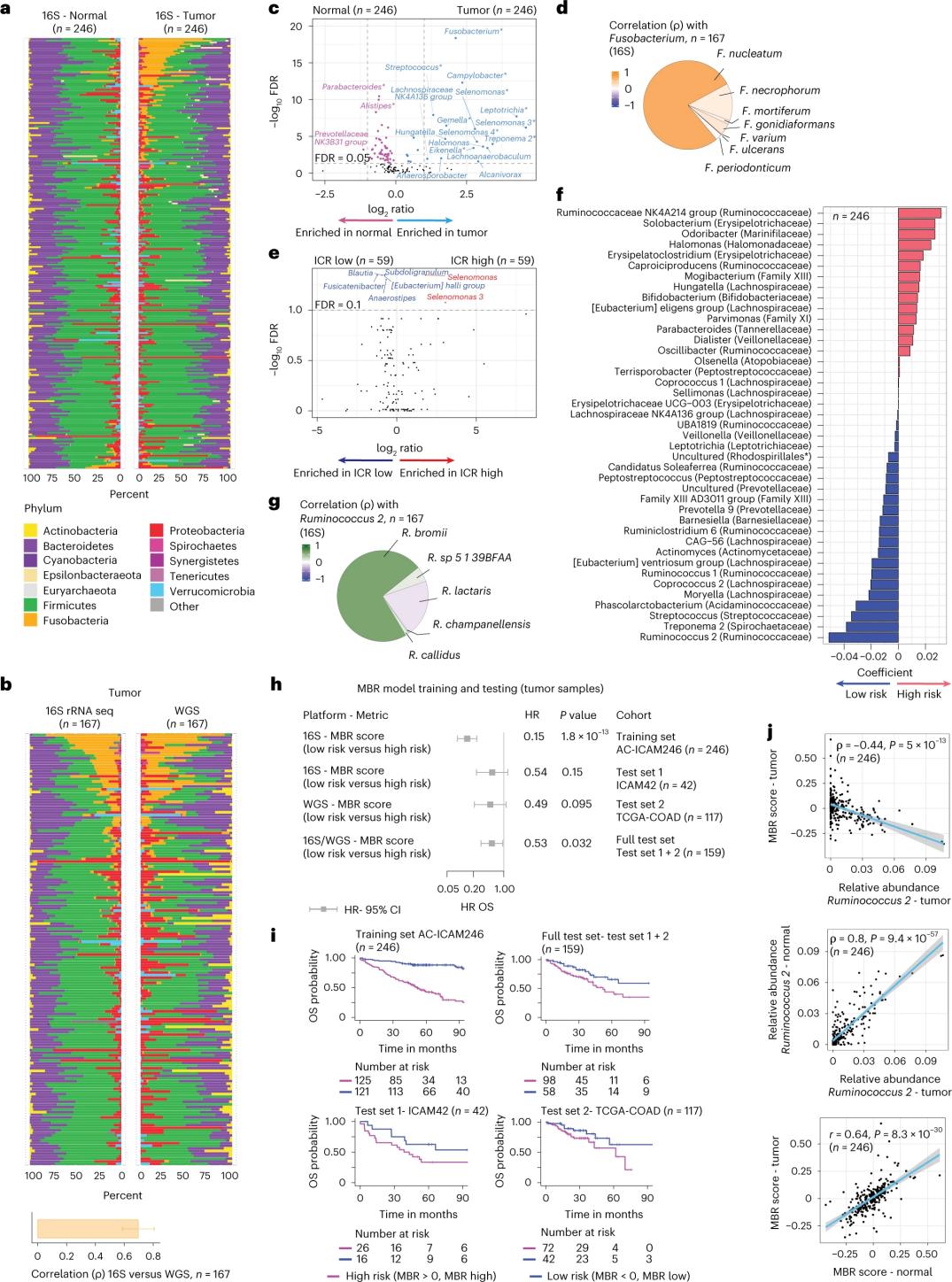
Obrázek 3. Mikrobiom v nádorových a zdravých tkáních a vztah k ICR a přežití pacientů.
Závěr
Multi-omický přístup použitý v této studii umožňuje důkladnou detekci a analýzu molekulárního podpisu imunitní odpovědi u kolorektálního karcinomu a odhaluje interakci mezi mikrobiomem a imunitním systémem. Hloubkové sekvenování TCR nádorových a zdravých tkání ukázalo, že prognostický účinek ICR může být způsoben jeho schopností zachytit nádorem obohacené a pravděpodobně i nádorově antigenně specifické klony T buněk.
Analýzou složení nádorového mikrobiomu pomocí sekvenování genu 16S rRNA ve vzorcích AC-ICAM tým identifikoval mikrobiomový podpis (MBR risk score) se silnou prognostickou hodnotou. Ačkoli tento podpis byl odvozen ze vzorků nádorů, existovala silná korelace mezi zdravým tlustým střevem a MBR score nádoru, což naznačuje, že tento podpis může zachycovat složení střevního mikrobiomu pacientů. Kombinací skóre ICR a MBR bylo možné identifikovat a validovat multiomický studentský biomarker, který predikuje přežití u pacientů s rakovinou tlustého střeva. Multiomický datový soubor studie poskytuje zdroj pro lepší pochopení biologie rakoviny tlustého střeva a pomáhá objevovat personalizované terapeutické přístupy.
Čas zveřejnění: 15. června 2023
 中文网站
中文网站